有机化学知识点(八)
第九章
羧酸
一
分类和命名
分类
1、按羧基连接的烃基:
①脂肪酸②脂环酸③芳香酸
2.按羧基数目:
①一元酸②二元酸③多元酸
命名
(1)俗名:
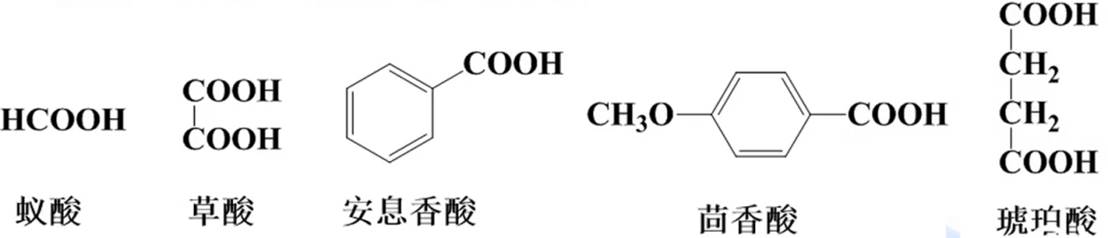
(2)系统命名法:
①有一个羧基:从羧基开始编号,与醛相似。
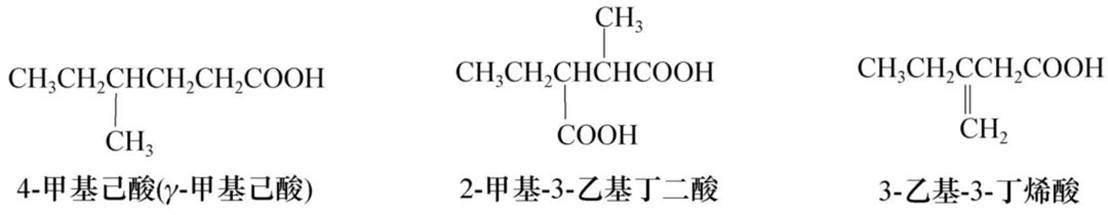
②有多个羧基:以有两个羧基的碳链为主链。
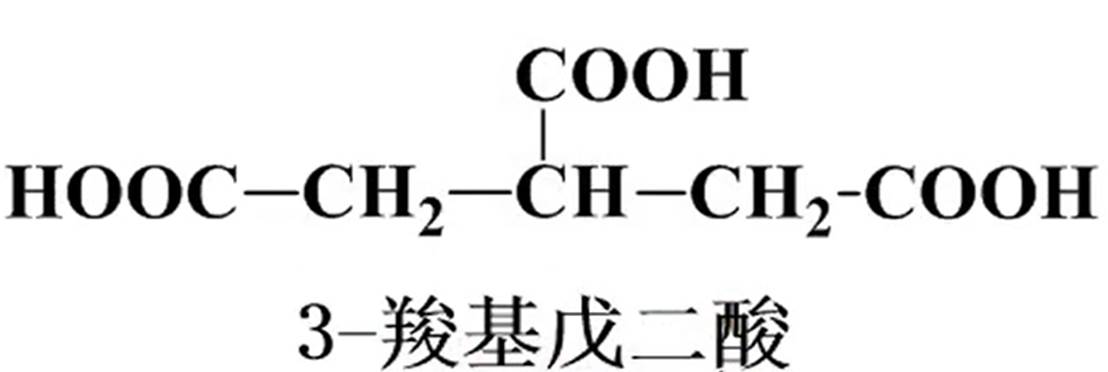
③芳香酸、脂环酸:芳环、脂肪环作为取代基。
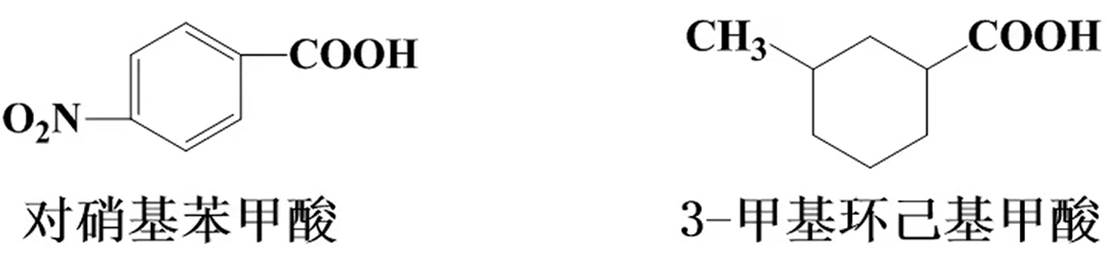
二
物理性质
①水溶性:羧基能与水分子形成氢键,含1~4个碳的饱和一元羧酸可与水混溶。几乎所有的羧酸盐都能溶于水。
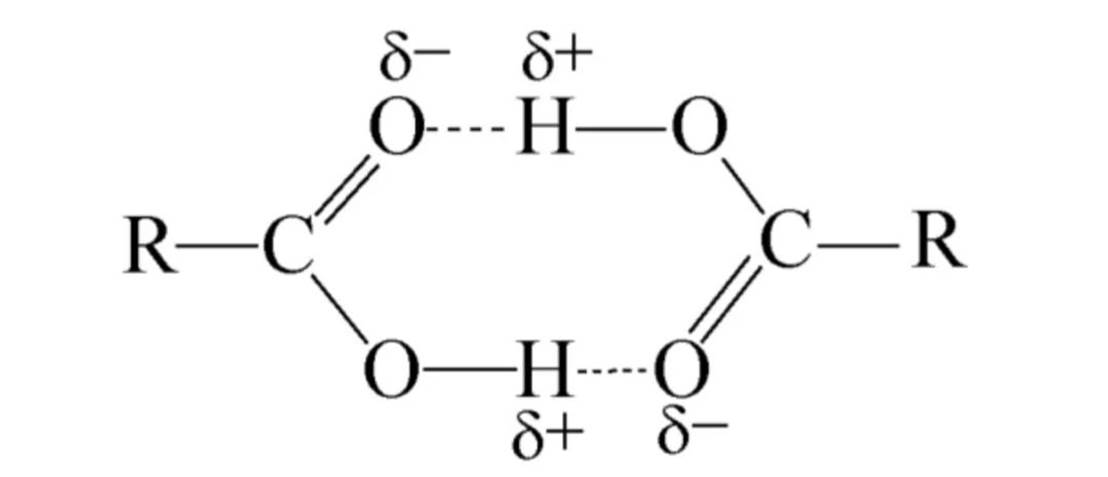
②沸点:羧酸分子间能形成一对氢键,使小分子羧酸之间互相缔合,因此羧酸的沸点比分子量相近的醇的沸点要高。
三
化学性质
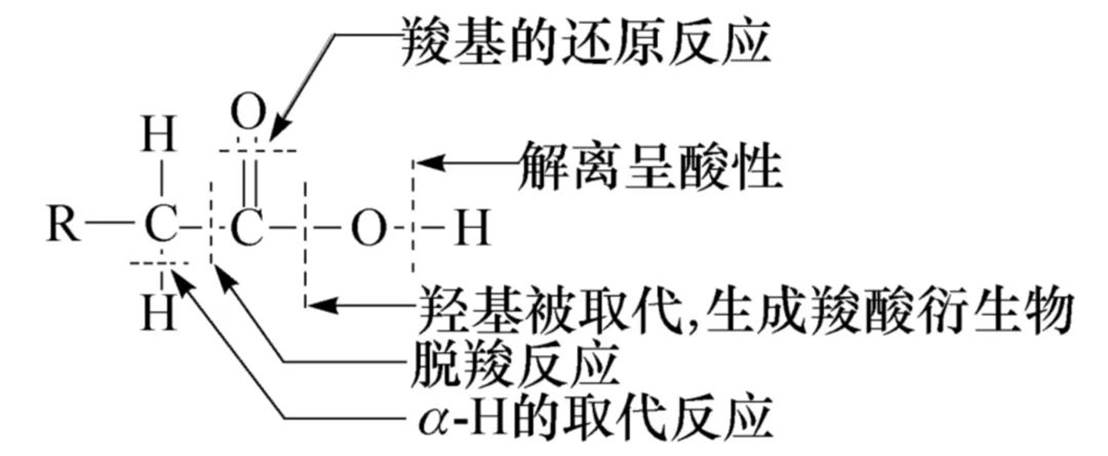
酸性
O-H键上电子云密度增大,则酸性减小。
羧酸衍生物的生成
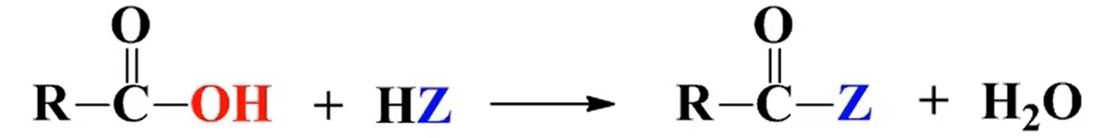
生成酰卤:
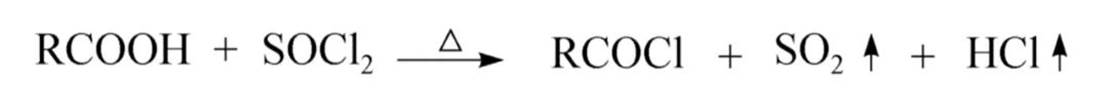
第三个反应的产物除酰卤外都是气体,易分离酰卤。
SOCl2:亚硫酰氯、氯化亚砜。
生成酸酐:
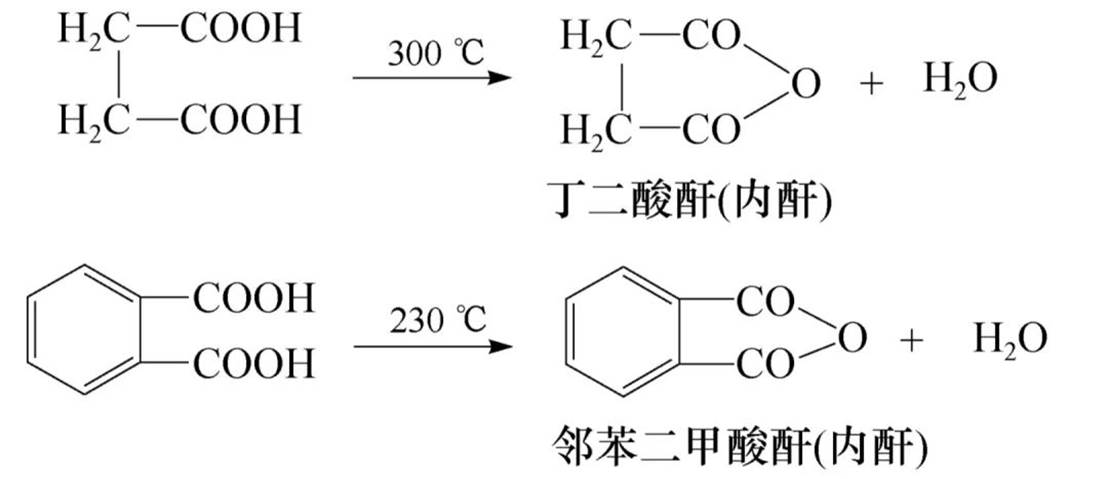
生成酯(酯化反应):
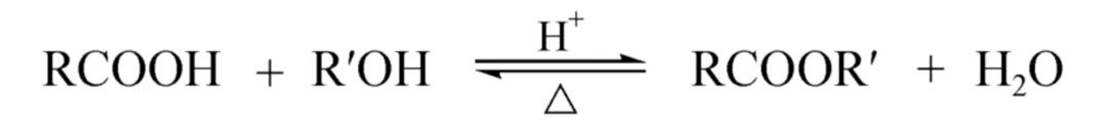
该反应的活性与反应物的空间位阻有关。
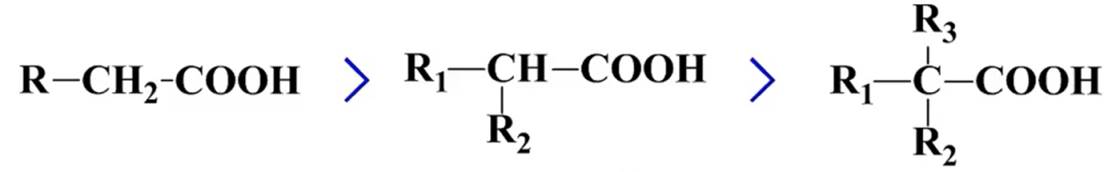
酰胺的生成:
羧酸与氨或胺作用得到羧酸的铵盐,然后铵盐在高温下分解失水得到酰胺。

还原反应
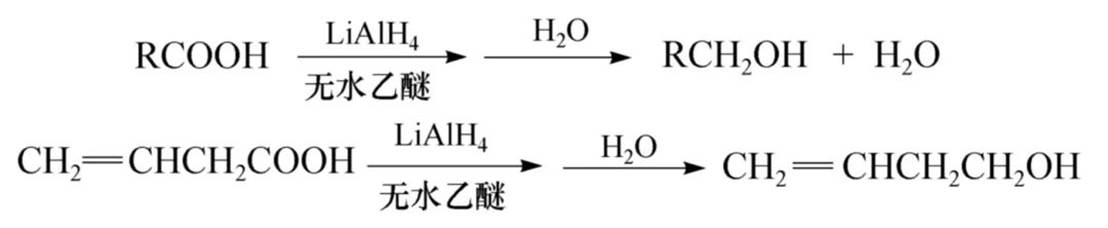
氢化铝锂(LiAIH4)是一种还原能力很强的试剂,用它还原酸,产量较高,而且对碳碳双键不起作用,因此不饱和酸可用LiAlH4还原为不饱和醇。
α-H的卤代
羧基是吸电子基团,由于诱导效应以及超共扼效应的影响,羧酸分子中的α-H比较活泼,在催化剂碘、红磷存在时,a-H可被氯、溴取代,继续反应可得二氯乙酸及三氯乙酸。例如
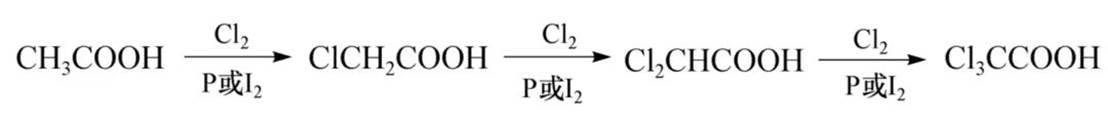
脱羧反应
一元酸难脱羧,但其盐与碱石灰共熔可脱羧:
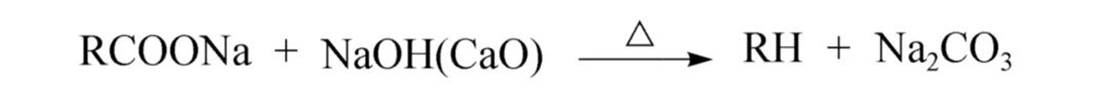
R为CH3时为实验室制甲烷;当α、β碳原子上有强吸电子基团时,容易脱羧。
二元酸中的乙二酸和丙二酸较易脱羧,直接加热即可脱形成一元酸。
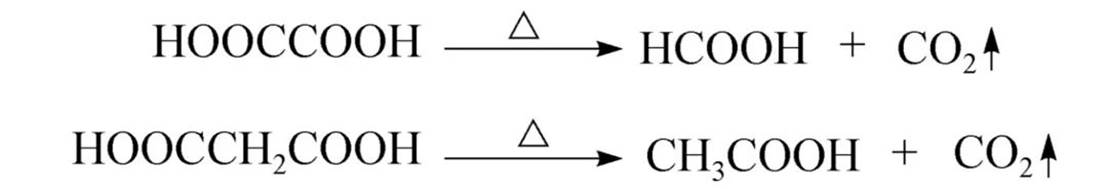
己二酸、庚二酸在氢氧化钡存在下加热,分子失水脱羧发生成环酮。
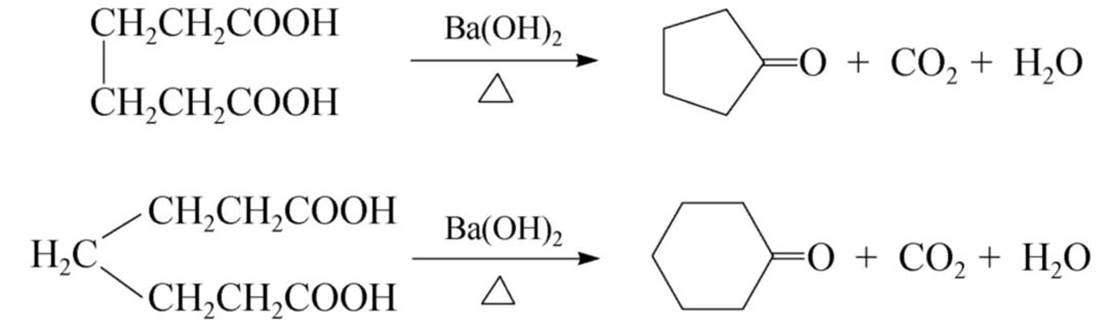
羧酸衍生物
一
命名
酰卤:酰基+卤素
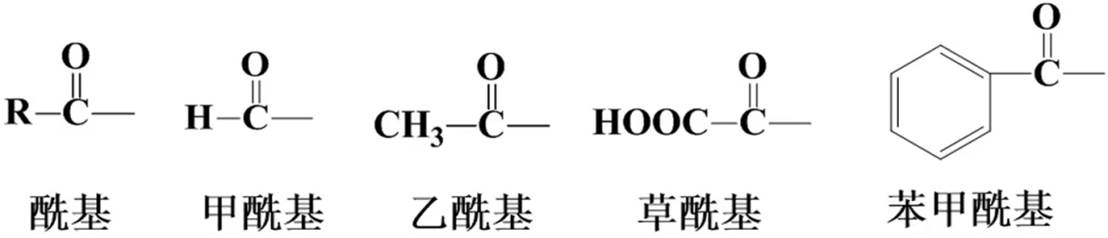
酸酐:
单纯酐:同一种酸形成的酐,称为“某酐”
混合酐:不同酸形成的酐,同时写出两个酸名称,小酸在前
内酐:二元酸分子内脱水
酯:酸在前,醇在后(某酸某酯)
酰胺:酸在前,胺在后,若氮上有取代基,在取代基的名称前冠以“N-”,表示取代基连在氮原子上。例如
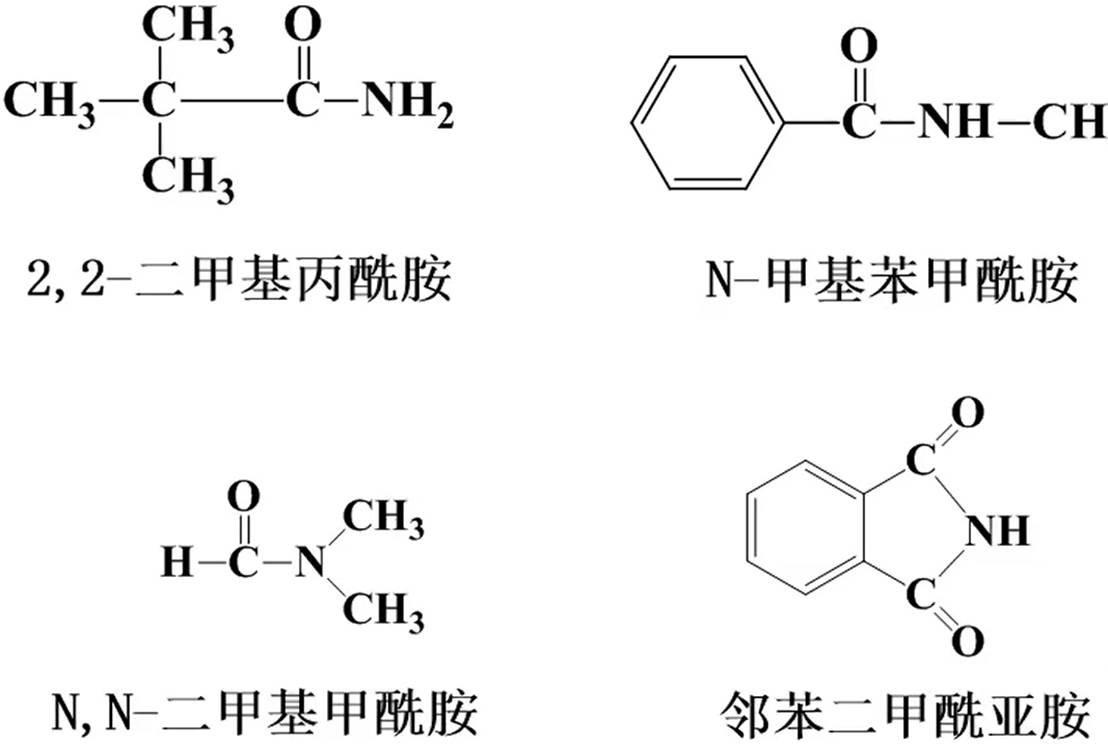
二
化学性质
水解反应
反应活性:
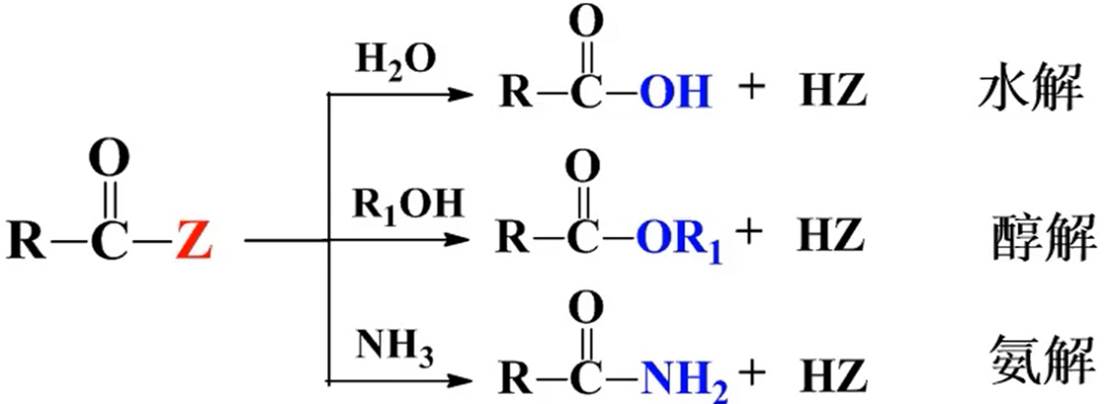
缩合反应(克莱森)
酯分子中的α-H比较活泼,在强碱如醇钠的作用下,可以和另一分子酯发生亲核加成消去反应生成β-酮酸酯
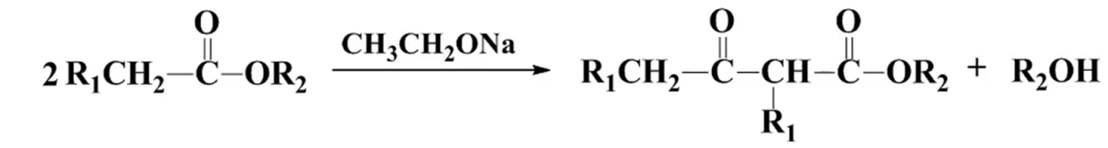
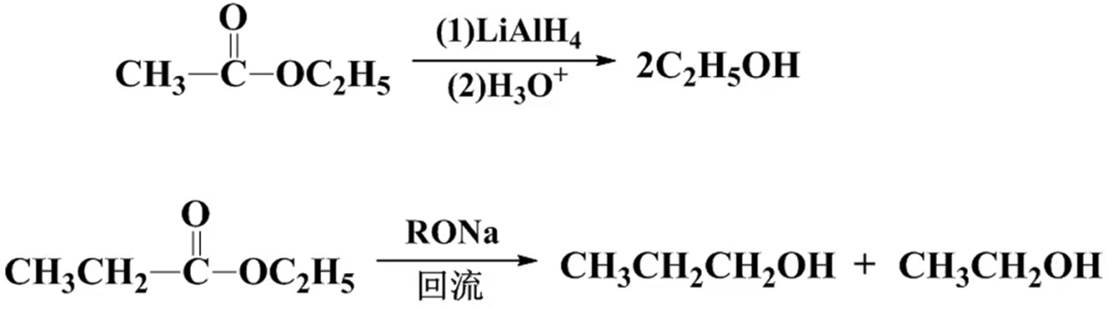
还原反应
酯的还原:
胺的酸碱性
酰胺分子显中性;
酰亚胺类分子中,由于亚氨基受两个直接相连的羰基影响,氮原子上电子云密度大大降低,失去质子的能力明显增加,从而使酰亚胺的酸性增强,通常显示出弱酸性。
酰胺的霍夫曼降级反应
伯酰胺的减碳反应:制备比原来少一个碳的伯胺。
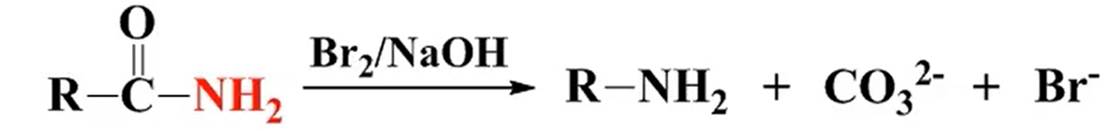
取代酸
一
化学性质
羟基酸
酸性:羟基距离羧基越近,吸电子诱导效应越强,酸性越强。
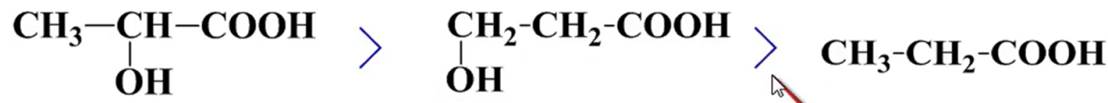
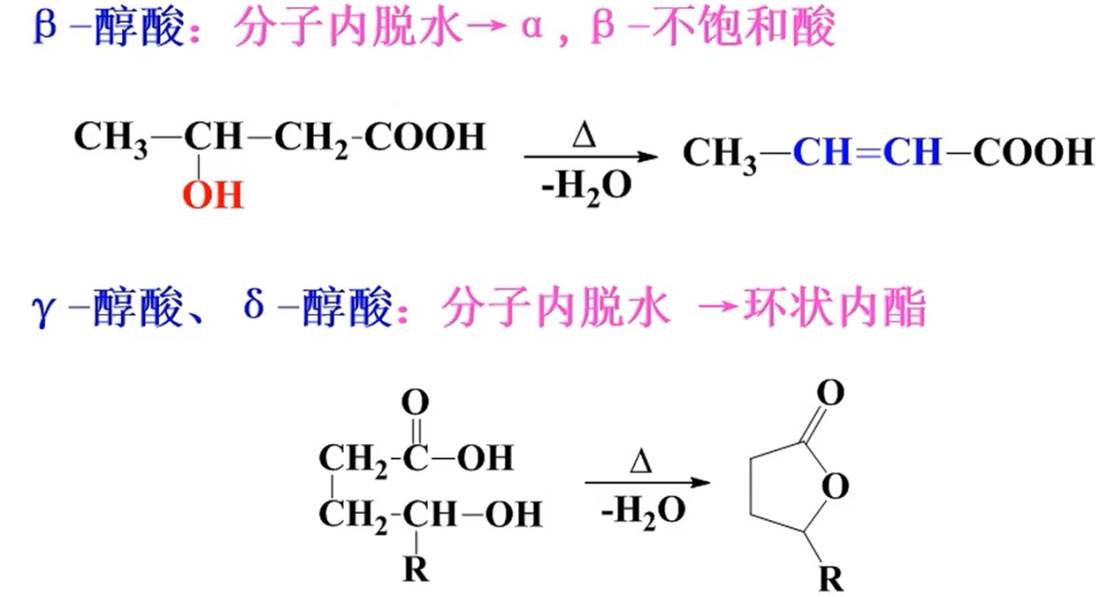
脱水反应:羟基与羧基距离不同,脱水方式也不同
羰基酸
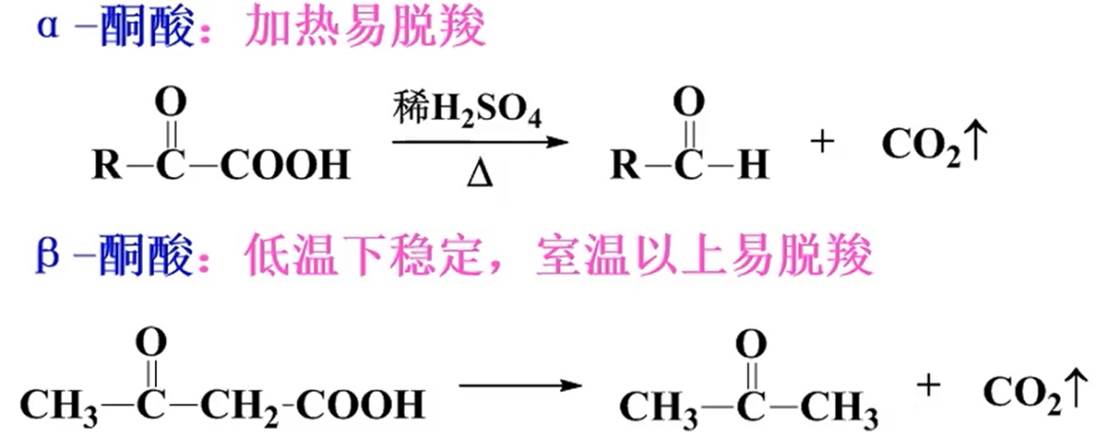
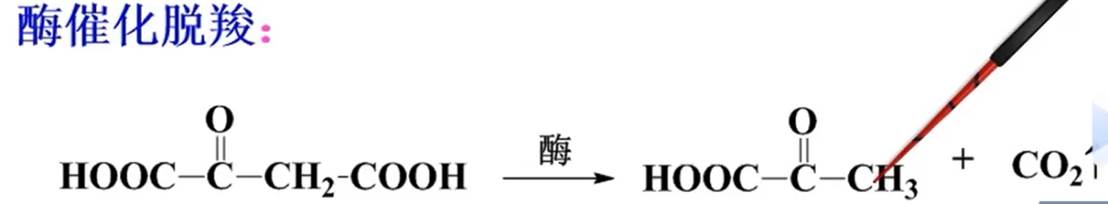
生物体内生成丙酮酸:
乙酰乙酸乙酯
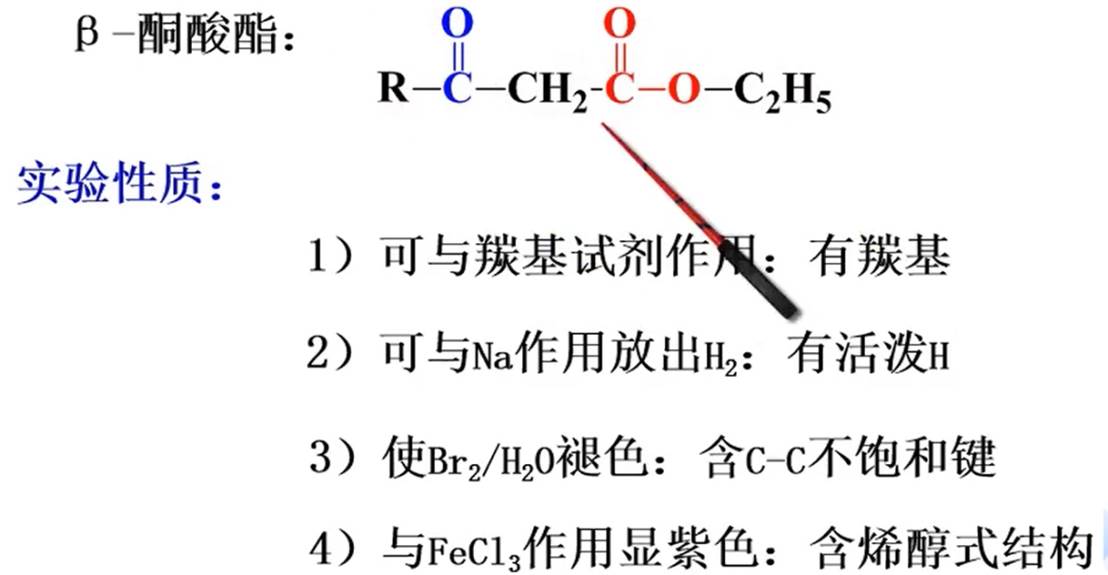
亚甲基H活泼可产生互变异构:
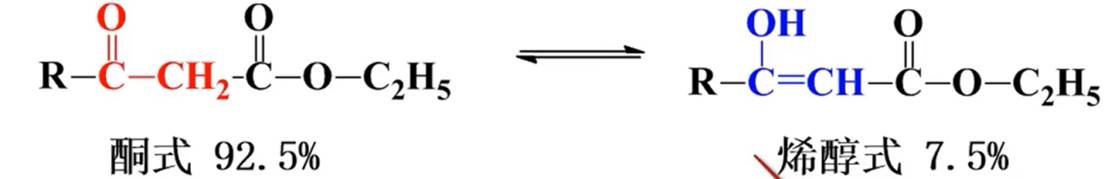
烯醇式稳定性制约因素:
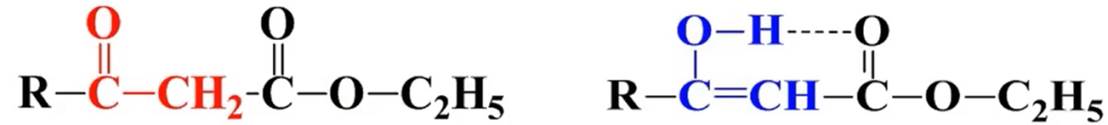
①羰基和酯基的-I效应,使得-CH2-的H活泼
②共轭体系增长,稳定性增大
③烯醇式结构中可形成六元环的分子内氢键
常见互变异构体系:
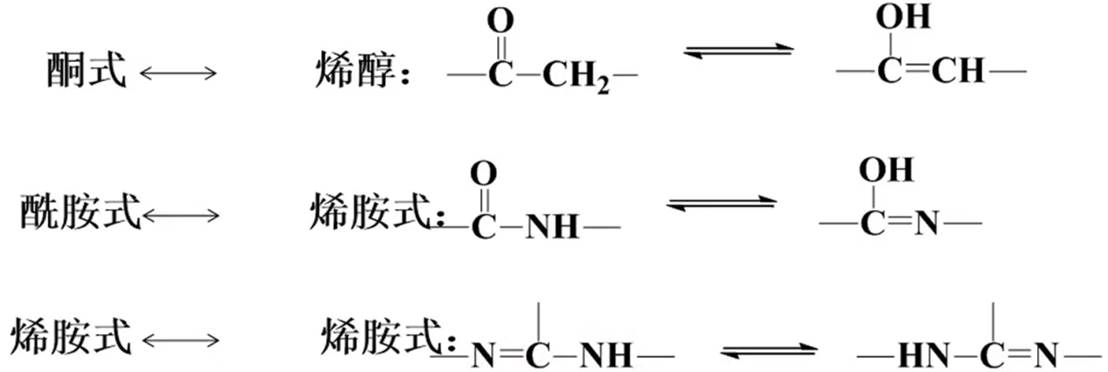

图文来源于学习通教材
