有机化学知识点(十一)
第十二章
单糖
一
结构
①单糖可分为醛糖和酮糖。
②把三碳糖称为丙醛糖和丙酮糖,四碳糖称为丁醛糖和丁酮糖,相应的醛糖和酮糖是同分异构体。
单糖的变旋现象和环状结构
有旋光性的化合物,放到溶液中,其比旋光度逐渐变化,最后达到一个稳定的平衡值的现象称为变旋现象。其他大部分单糖,如:果糖、甘露糖、核糖等也都有变旋现象。
五元环和六元环最容易形成。C1羰基与C5上的羟基发生加成反应,生成六元环状的半缩醛式结构。
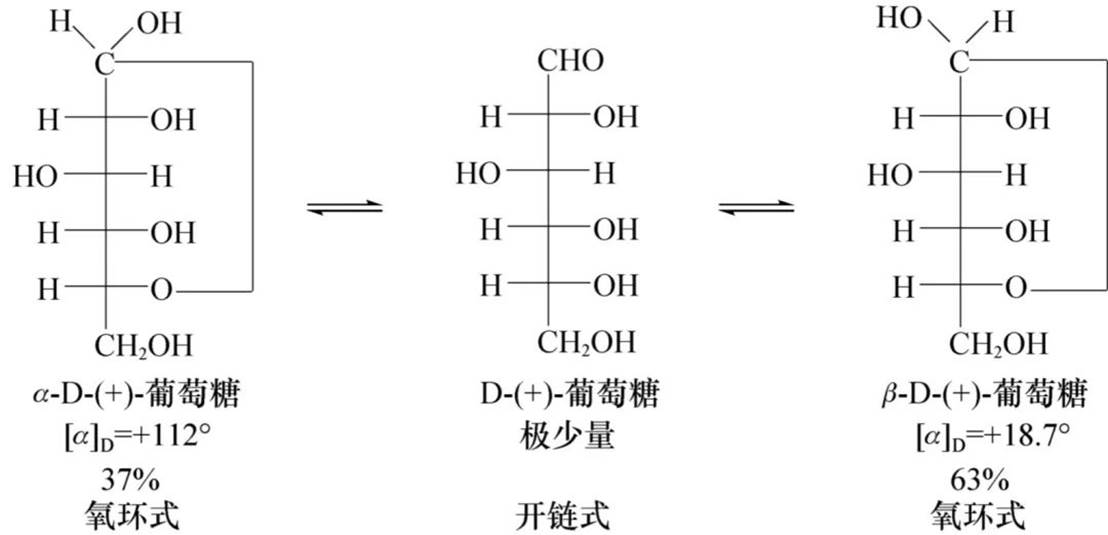
在两种氧环式结构中,C1成为新的手性中心,有两种异构体,其中半缩醛羟基与C5上的羟基在同一侧的称为α型,不在同一侧的称为β型。
两种异构体中只有C1构型不同,其他手性碳的构型都相同的异构体称为C1-差向异构体,也称为端基异构体或异头物。
单糖的哈沃斯式
①首先水平画出表示氧环式结构的六元环,其中氧原子放在右后方,环上碳原子按顺时针方向排列。
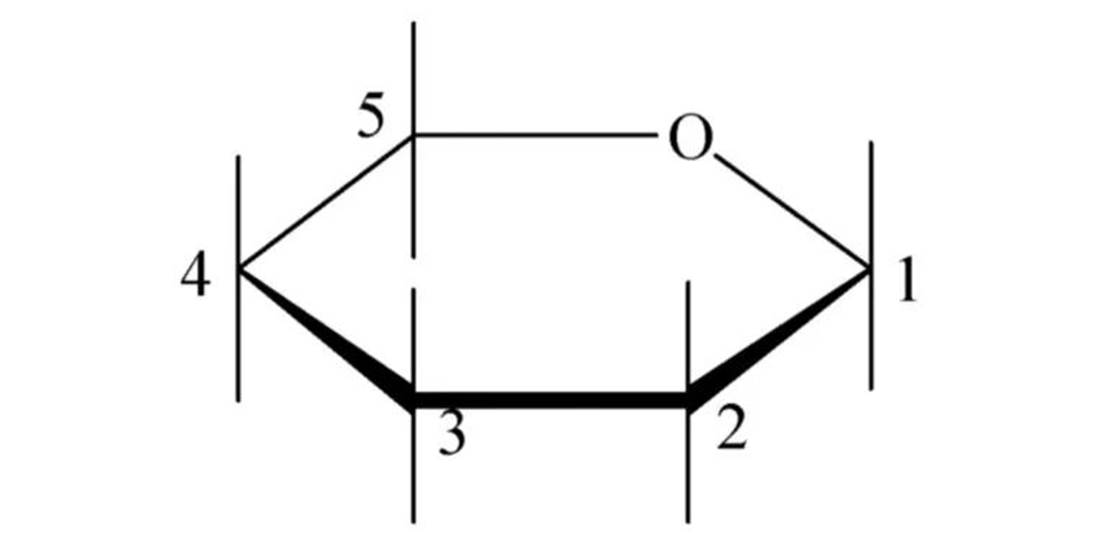
②将费歇尔投影式中竖线左边的基团写在哈沃斯式环平面的上面,右边的基团写在下面,即遵循“左上右下”的原则。
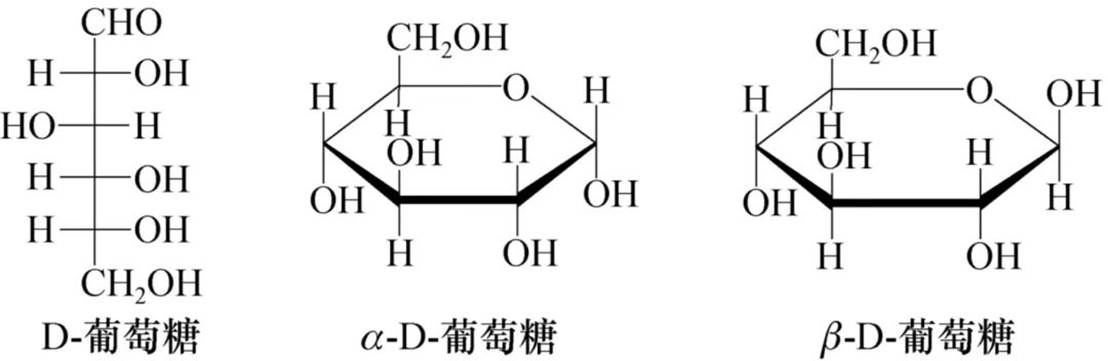
③D-型糖的尾基(—CH2OH)写在上面,L-型糖的尾基写在下面。
④半缩醛羟基的位置同样遵循“左上右下”的原则,如D-型糖中,α型的半缩醛羟基写在下面,β型的半缩醛羟基写在上面,而L-型糖则相反。
水平放置的五元环氧原子放在后面。有时为了方便可以将换环平面旋转,有时也可以翻转,但排序按照逆时针排序。
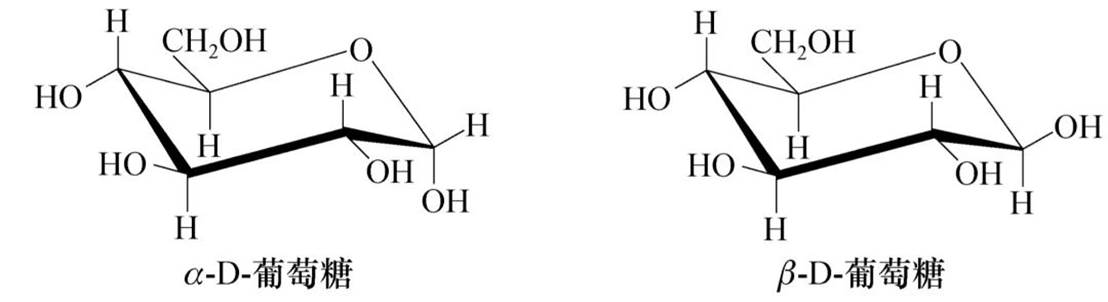
单糖的构象
从构象式可以看出,在型中所有较大基团都占据e键,而在α型中C1上的半缩醛羟基只能占据a键,所以β型比α型更稳定,在变旋平衡体系中β-D-葡萄糖占比例较大(63%)。
二
物理性质
单糖都是无色结晶,有吸湿性,极易溶于水,可溶于乙醇,不易溶解于乙醚、丙酮、苯等有机溶剂,但能够溶于吡啶。
单糖(除丙酮糖外)都有旋光性且大多具有变旋现象。
单糖和二糖都有甜味,各种糖的甜度不同。
三
化学性质
羰基与羟基相互作用会产生一些新的性质
差向异构化作用
在碱性条件下的异构化:
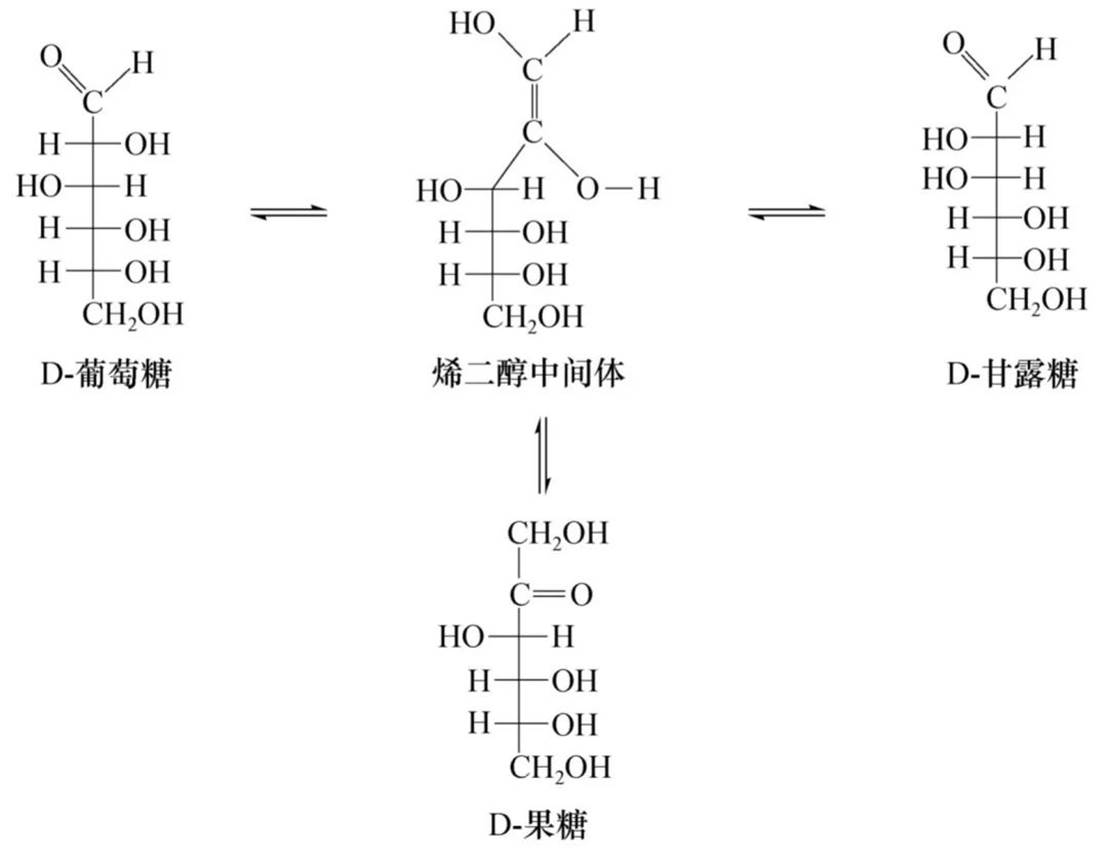
D-葡萄糖和D-甘露糖只有C2构型不同,其他手性碳构型都相同,称为C2-差向异构体
氧化反应
碱性条件下的氧化:
由于酮糖和醛糖在碱性条件下发生差向异构化作用而相互转化,因此醛糖和酮糖都可以被弱氧化剂如土伦试剂、费林试剂或本尼迪特试剂氧化,生成单质银或氧化亚铜沉淀。所有的单糖都具有还原性,称为还原性糖。
酸性条件下的氧化:
酸性条件下没有差向异构化作用,因此醛糖和酮糖性质不同。酸性条件下,溴水只能氧化醛糖而不能氧化酮糖,该反应可用于鉴别醛糖和酮糖,也可用于糖酸的制备。
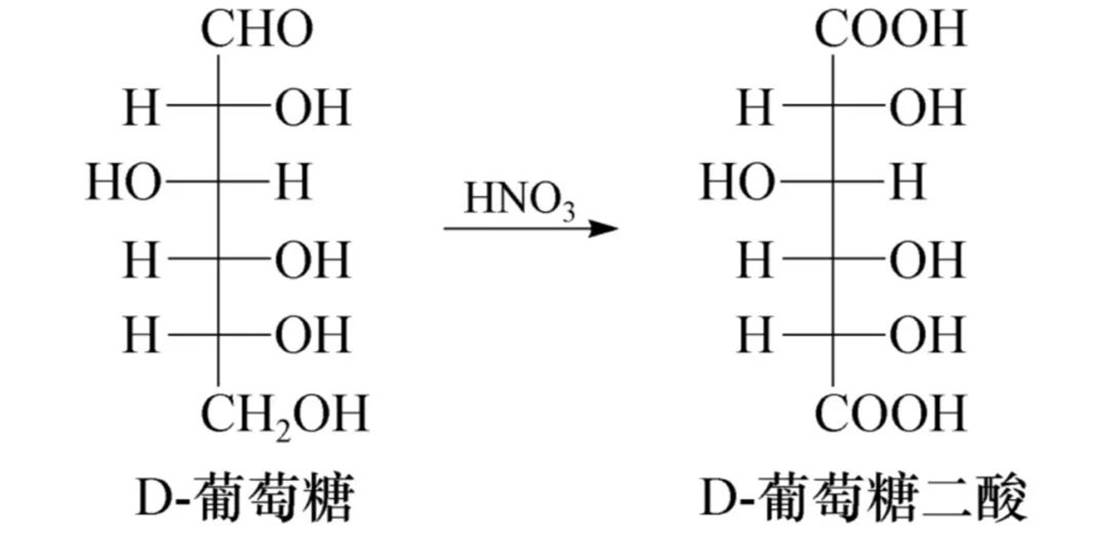
更强的氧化剂硝酸不仅可以氧化醛基,也可以氧化尾基(—CH.OH),生成糖二酸。
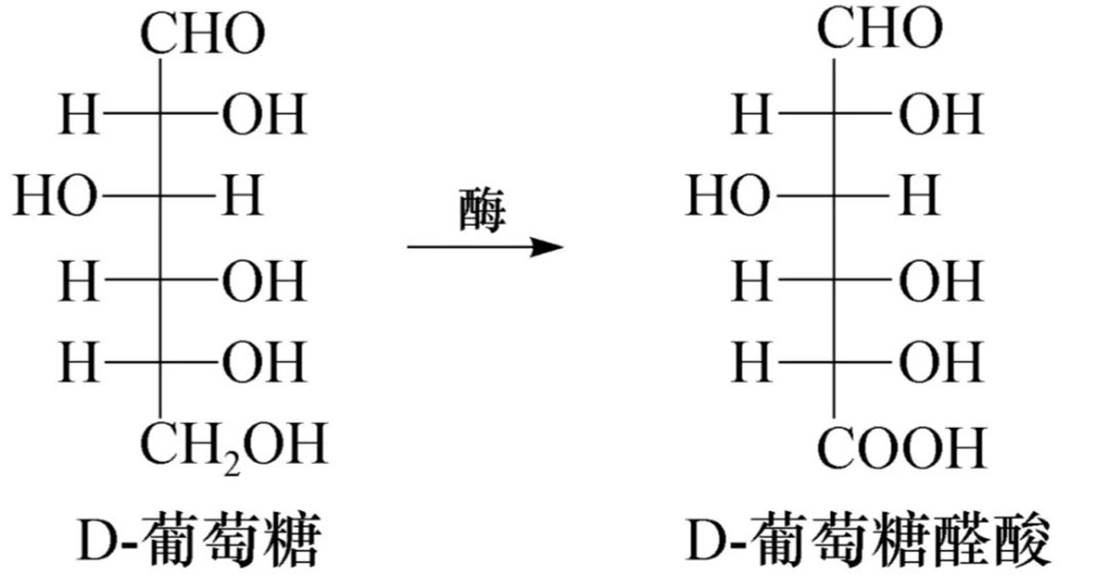
在生物体内酶的作用下,某些单糖如葡萄糖、半乳糖的羟甲基也可被氧化成羧基,而醛基保持不变,生成相应的糖醛酸。
还原反应
还原后,单糖分子的手性可能发生变化。例如,D-半乳糖还原后生成了内消旋的糖醇,而D-葡萄糖的还原产物D-山梨醇仍有手性。
成脎(sa)反应
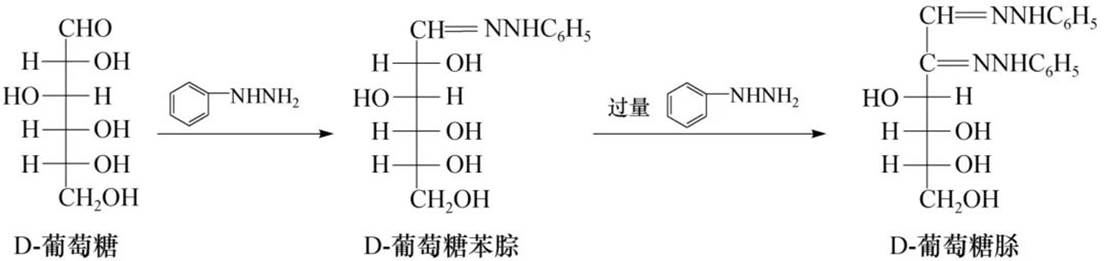
单糖分子中的基可以与苯胖作用生成糖苯腙,过量的苯肼将其α-位的羟基氧化成羰基,再与苯肼作用,最终生成糖脎。
成酯和成苷反应
成酯反应:
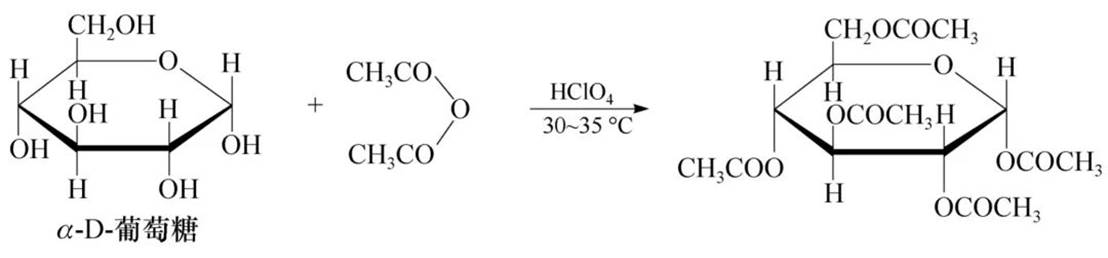
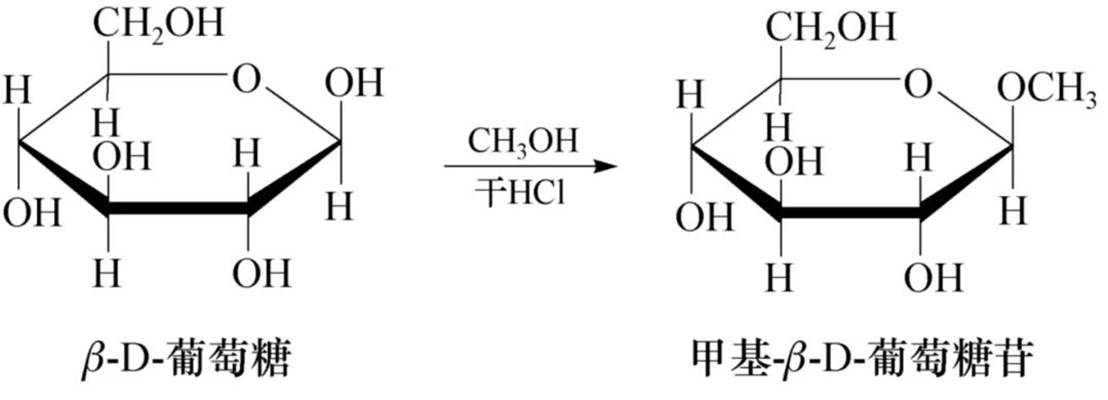
成苷反应:
单糖环状结构中的半缩醛羟基也称为苷羟基,能与含有羟基、巯基、亚氨基等基团的化合物脱水生成缩醛型化合物,这种化合物称为糖苷,该反应称为成苷反应。其中糖的部分称为糖基,非糖部分称为配基或苷元,糖基与配基之间相连的键称为苷键。
显色反应
(1)莫力许反应。在浓硫酸存在下,所有的糖(包括单糖、多糖)都能与α-萘酚反应生成紫色物质。该反应也称为α-萘酚反应,是糖类化合物定性鉴定的常用方法之一。
(2)蒽酮反应。在浓硫酸存在下,所有的糖(包括单糖、多糖)都能与蒽酮反应生成蓝绿色物质。该反应可用于糖类的定性鉴定,也可用于比色法进行糖类的定量分析。
(3)西列瓦诺夫反应。醛糖、酮糖与间苯二酚的浓盐酸溶液共热,酮糖在2min内生成有色物质,醛糖在2min内不显色,果糖显红色,戊酮糖显蓝至绿色。该反应也称为间苯二酚反应,用于区别醛糖和酮糖。
(4)皮阿尔反应。在浓盐酸存在下,戊糖与5-甲基-1,3-苯二酚反应生成绿色物质。该反应用于鉴别戊糖。
(5)狄斯克反应。在乙酸与浓硫酸混合液中,脱氧核糖与二苯胺反应生成蓝色物质。此反应用于鉴别脱氧核糖。
四
重要的单糖
自然界已发现的单糖主要是戊糖和己糖。常见的戊糖有D-核糖、D-2-脱氧核糖、D-木糖和L-阿拉伯糖。它们都是醛糖,以多糖或苷的形式存在于动植物中。常见的己糖有D-葡萄糖、D-甘露糖、D-半乳糖和D-果糖,后者为酮糖。己糖以游离或结合的形式存在于动植物中。
二糖
一
还原性二糖
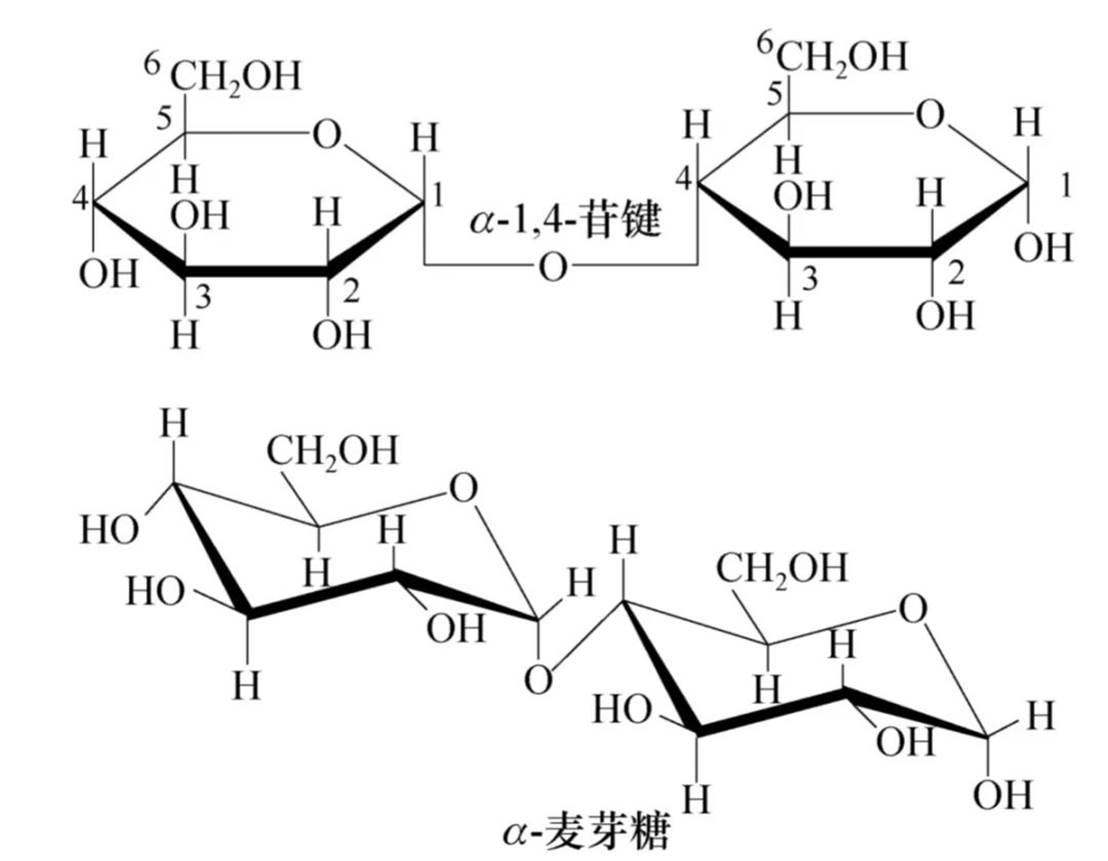
麦芽糖
两分子D-葡萄糖通过α-1,4-苷键相连,分子中仍保留一个半缩醛羟基,可通过开链和环状结构式相互转变,产生变旋现象。
麦芽糖能被弱氧化剂土伦试剂、菲林试剂以及溴水、硝酸等氧化,能与苯作用生成现象。
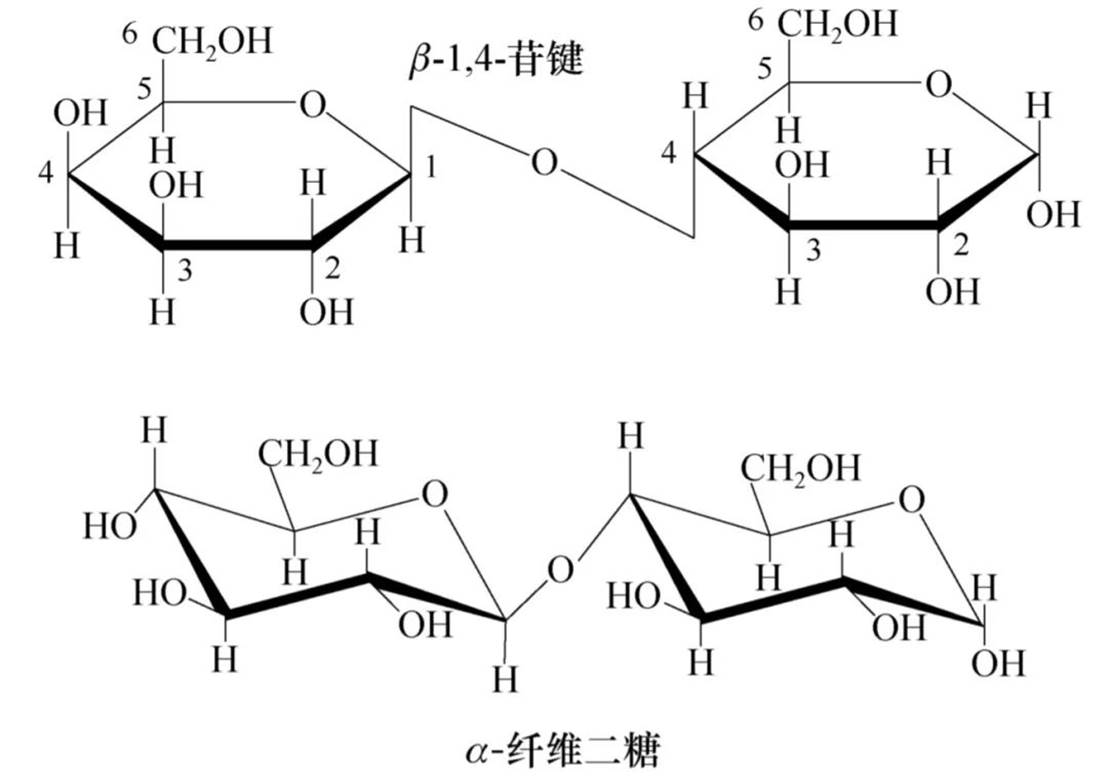
纤维二糖
纤维二糖可以水解成两分子D-葡萄糖,但不同于麦芽糖的是,水解纤维二糖必须用葡萄糖甘酶(苦杏仁酶),表明两分子葡萄糖间是以β-1,4-键相连。
化学性质与单糖相似。
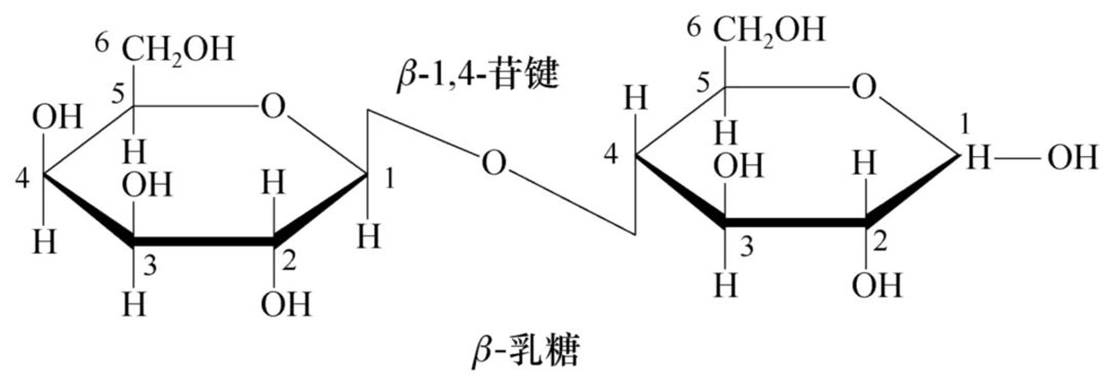
乳糖
乳糖经酸或苦杏仁酶水解得到一分子D-半乳糖和一分子D葡萄糖,它是由β-D-半乳糖的半缩醛羟基与D-葡萄糖C4上的醇羟基脱水,通过β-1,4-苷键缩合而成。
二
非还原性二糖
非还原性二糖是两分子单糖间均以半缩醛羟基缩合,形成的二糖分子中没有半缩醛羟基,因此没有变旋现象,没有还原性,不能被弱氧化剂氧化,也不能与苯生成糖脎。
蔗糖
蔗糖是由一分子α-D-葡萄糖C1上的半缩醛基与另一分子β-D-果糖C2上的半缩醛泾基脱去一分子水,通过α,β-1,2-苷键连接而成的。
海藻糖
它是由两分子α-D-葡萄糖的半缩醛羟基通过α-1,1-苷键缩合而成,分子中没有半缩醛羟基,属于非还原性二糖。
多糖
一
淀粉
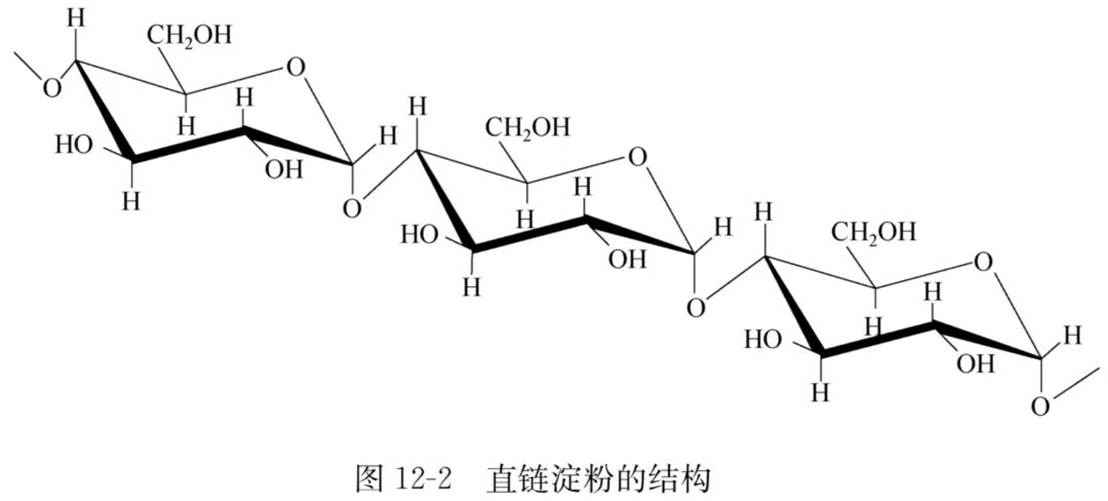
直链淀粉
直链淀粉并非直线形结构,而是通过分子内氢键使链卷曲成螺环状,螺环中间的空隙刚好可以容纳碘分子进入,形成深蓝色的包合物。此显色反应常用于淀粉的检验。
直链淀粉能溶于热水,可以被淀粉酶全部水解为麦芽糖。
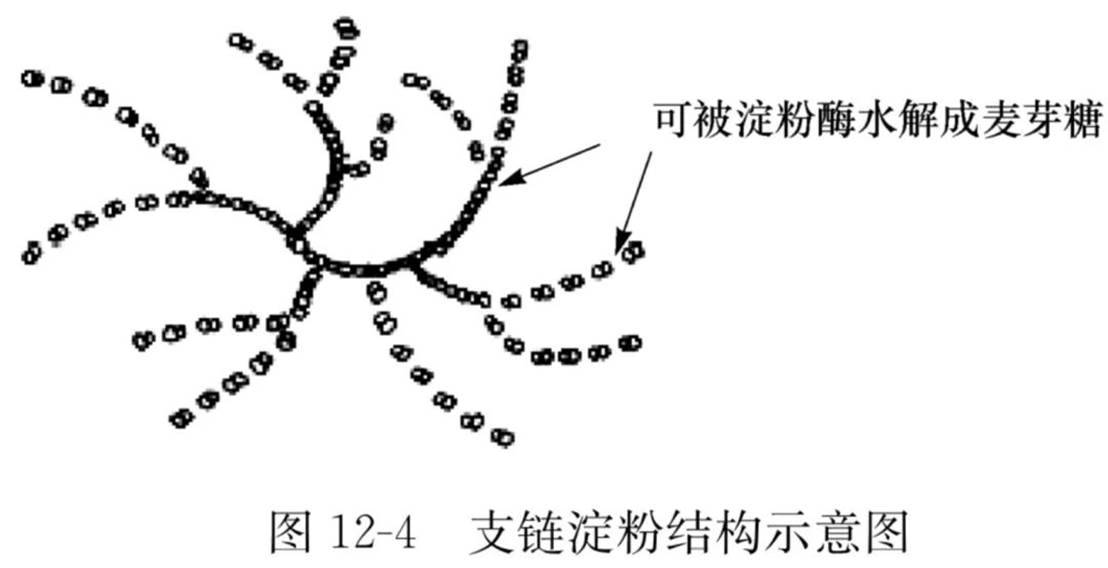
支链淀粉
支链淀粉分子中可含百万个α-D葡萄糖单位,比直链淀粉分子更大,支链淀粉不溶于水,在热水中吸水膨胀形成黏稠糊状。支链淀粉遇碘可显紫红色,在淀粉酶作用下只有约60%被水解成麦芽糖。
二
纤维素
纤维素是由几千乃至上万个β-D葡萄糖通过β-1,4-苷键连成的链状高聚物,没有分支,用40%盐酸水解可得到D-葡萄糖,用酸小心水解可得到纤维二糖。。
纤维素无味,常温下既不溶于水,又不溶于一般的有机溶剂,如乙醇、乙醚、丙酮、苯等,但可溶于氢氧化铜的氨溶液、氯化锌的盐酸溶液、二硫化碳和氢氧化钠中,形成黏稠的溶胶。

图文来源于学习通教材
